Los triacilglicéridos y éteres etílicos en los Omega-3
Seguramente ya sabrás que la forma de administración de suplemento alimenticio o un fármaco es determinante a la hora de lograr un efecto en nuestro organismo. Y efectivamente, en el caso de los ácidos grasos Omega-3, esto se cumple.
En este post te contamos como obtener el máximo beneficio (rendimiento) de tus suplementos con omega-3 respondiendo a 3 preguntas muy básicas que tenemos que conocer acerca de ellos.
1º) Y tú, ¿Cómo te tomas el Omega-3? ¿En ayunas o con las comidas?
Este aspecto, como te vamos a contar, es de excepcional importancia para lograr su máximo beneficio. Tal vez te hayas preguntado en alguna ocasión porqué es necesario tomar los suplementos alimenticios con las comidas. Pues bien, la razón de hacerlo coincidir en el tiempo no es para que no te olvides de tomarlo (aunque también puede ser de ayuda si somos un poco despistados), sino porque su absorción a nivel intestinal es muy superior comparado con la que obtendríamos si lo tomásemos en ayunas.
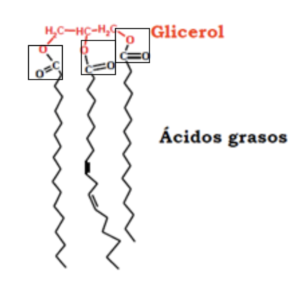
Sin embargo, las células de nuestra mucosa intestinal son incapaces de absorber los TAG, por ello éstos tienen que ser descompuestos en sus elementos constituyentes. Para que estos elementos se disocien necesitan romper los enlaces éster y liberar los ácidos grasos constituyentes, los cuáles son absorbidos por las células intestinales. Esta reacción se lleva a cabo gracias a la acción de una enzima conocida como «lipasa pancreática», una de las herramientas de la que dispone el jugo pancreático y que posibilita la digestión de las grasas con la ayuda de las sales biliares, quienes permiten «emulsionar» las grasas y «hacerlas accesibles» para la actuación de la lipasa. La lipasa pancreática hidroliza los enlaces éster (rompe los enlaces con la participación de una molécula de agua) los enlaces ésteres de la posición 1 y 3 del ácido graso (α y γ en el esquema inferior), generando dos ácidos grasos libres y una molécula de glicerol con un ácido graso esterificado en la posición central, 2-monoacilglicerol (imagen inferior) [1].


Aquí es cuando los ácidos grasos procedentes de la dieta, y los omega-3, están disponibles para ser utilizados por las células de nuestro organismo. Esto es lo que se conoce como la biodisponibilidad, es decir, la fracción de ácidos grasos asimilados y funcionalmente disponibles para nuestras células.
Volviendo a nuestra pregunta inicial, ¿por qué se absorben mejor los omega-3 si se toman con las comidas? Para poder entender esto, tenemos que adentrarnos un poco en nuestra fisiología, concretamente en los mecanismos que rigen la digestión.
El proceso de la digestión de las grasas comienza en la boca, donde los primeros TAG son hidrolizados por la lipasa lingual. Esta enzima, liberada durante la masticación y la presencia de TAG en la boca, es responsable de generar una pequeña proporción de ácidos grasos libres. Aunque la eficiencia de esta enzima es muy restringida, su actuación ante la presencia de TAG es decisiva para que la absorción de estos primeros ácidos grasos liberen una hormona llamada «colecistoquinina», responsable de inducir la liberación del jugo pancreático y la bilis almacenada en la vesícula biliar [3, 4]. El jugo pancreático contiene toda la colección de las principales enzimas digestivas (proteasas como tripsina y quimotripsina, glucosidasas, nucleasas, lipasas…), entre las que se encuentra la lipasa pancreática, la principal enzima al cargo de descomponer los TAG en sus formas absorbibles (ácidos grasos y 2-monoacilglicerol).
De este modo, la presencia de grasas en la boca y la actuación de la lipasa lingual en primer lugar dispara el proceso de digestión de TAG a mayor escala en el intestino delgado, facilitando de este modo la actuación de la lipasa pancreática y la absorción de los omega-3.
Por esta razón, y en consonancia con lo descrito por varios estudios científicos [2, 5-7] para lograr unos niveles óptimos de biodisponibilidad de omega-3 en plasma, es necesario tomarlos con las comidas, ya que éstas siempre van a contener las cantidades necesarias de TAG para desencadenar el proceso.
2º) ¿Por qué las empresas suelen administrar los omega-3 en forma de esteres etílicos en lugar de Triacilglicéridos?
Para poder responder a esta pregunta, es necesario conocer:
¿En qué consisten el proceso de obtención, purificación y concentración de los ácidos grasos Omega-3?
1.En primer lugar, una vez obtenido el aceite de pescado, es necesario su descontaminación mediante destilación molecular. Este proceso permite obtener un mayor grado de pureza cuantos más ciclos se efectúen.
2. A continuación es necesario transformar los TAG constituyentes del aceite en ésteres etílicos (EE), en una reacción que se conoce como «transesterificación por alcoholisis, esto es romper los enlaces éster de los TAG y formar nuevos enlaces éster con etanol (esquema inferior). Esta reacción se realiza utilizando etanol como reactivo y un catalizador, obteniendo los denominados EE con concentraciones en DHA y EPA superiores al 30%.

Sin embargo, para obtener concentraciones de Omega-3 superiores al 90% son necesarias otras técnicas de fraccionamiento y varios ciclos de destilación molecular generan estrés térmico.
4. Esto se consigue separando los EE mediante cromatografía de líquidos en fase supercrítica con CO2 (SFC, por sus siglas en inglés) . Esta técnica, combina el poder de separación y concentración de la cromatografía con las ventajas de utilizar una fase líquida supercrítica (CO2 supercrítico). Debiéndose a que el CO2 en esta fase se comporta como un buen disolvente orgánico, capaz de solubilizar los EE, sin tener toxicidad. De esta forma se pueden recoger fracciones enriquecidas con hasta un 98% de Omega-3 [8].
5. Sin embargo, y como veremos en el próximo punto, para que los omega-3 sean fácilmente absorbidos, y «accesibles» para nuestras células, esto es, biodisponibles, es necesario ingerirlos en la forma Triacilglicérido re-esterificado (TAG re). Por esta razón, es determinante una última etapa de transesterificación que permita disponer de los TAG en formato re-esterificado, lo que garantiza una buena biodisponibilidad de Omega-3, con un alto índice de pureza y concentración.
Evidentemente, comercializar un suplemento alimenticio de omega-3 con el formato de EE requiere una etapa menos en el proceso de elaboración, lo que permite abaratar costes. Sin embargo, como os explicamos a continuación, su «biodisponibilidad«, es decir, la proporción de estos ácidos grasos que son asimilables por nuestras células, es muy reducida en comparación a la que se obtiene cuando se ingieren en la forma de TAG re.
3º) ¿Cuál es la biodisponibilidad en el tiempo de los TAG vs EE?
Hasta aquí, ya sabemos que los Omega-3 se absorben mucho mejor cuando se ingieren con las comidas, y especialmente en forma de TAG. Sin embargo, para poder comparar los niveles plasmáticos circulantes de éstos ácidos grasos en el tiempo, hemos de entender el concepto de «biodisponibilidad». Se trata de un parámetro farmacocinético que relaciona la cantidad de un fármaco o suplemento alimenticio absorbido con relación a la cantidad ingerida en términos porcentuales. Gráficamente, representa el área bajo la curva de la representación de concentración plasmática de la sustancia en cuestión frente al tiempo [9]. Evidentemente, la biodisponibilidad es tanto mayor cuanto mayor sea la cantidad inicial absorbida (proceso clave) y menor o más lentos sean procesos como el metabolismo y la eliminación.
Por esta razón, es fácil entender como algunos suplementos que contienen una gran cantidad de Omega-3 pueden tener una biodisponibilidad muy baja, especialmente si lo es su absorción. Precisamente, esto es lo que sucede cuando los suplementos aportan los omega-3 en la forma de EE. Esto se debe a que la absorción de los ácidos omega-3 es estrictamente dependiente de la actuación de la lipasa pancreática. Esta enzima, como cualquier otra, es específica para un sustrato o grupo reducido de moléculas, por lo que la generación del producto de interés, ácidos grasos omega-3 libres, depende de la «especificidad» de la enzima por los diferentes sustratos. En este sentido, la lipasa pancreática cataliza el proceso de hidrólisis de enlaces ésteres de forma selectiva cuando éstos forman parte de un TAG, mientras que su acción sobre otros sustratos, como los EE es muy reducida.
Los resultados se conocen desde hace más de treinta años, cuando Lawson y colaboradores (1988) manifestaron las concentraciones plasmáticas de EPA en el tiempo.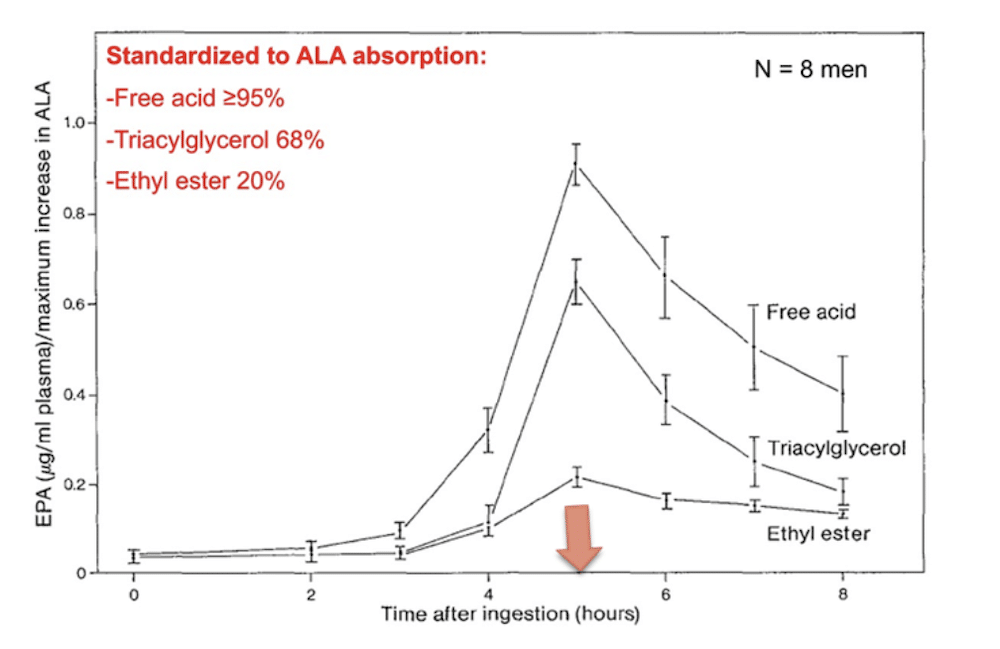
Al aplicar TGA para administrar EPA, se observo que la biodisponibilidad mantenía niveles muy altos (próximos al 70%), para administrarse como ácido graso libre. Sin embargo, la biodisponibilidad de EPA cae a niveles mínimos cuando se administra en forma de EE (inferior al 20%), una formulación que es ampliamente utilizada en muchos suplementos de Omega-3 [5].
¿Qué conclusión podemos extraer de estos datos? Los datos hablan por sí mismos. La biodisponibilidad de Omega-3 es muy superior cuando éstos se ingieren en la forma de TAG mientras que su absorción, y por lo tanto la biodisponibilidad de éstos es mínima cuando se administran como ésteres etílicos [2, 5, 6]. Esto implica que la fracción de Omega-3 disponible para nuestras células es mayor y durante más tiempo cuando estos son administrados como TAG.
Entonces, ¿Por qué no tomarlos como ácidos grasos libres?
Su biodisponibilidad sería máxima si formaran parte de lípidos complejos, pero su inestabilidad frente a la oxidación descarta esta posibilidad.
Bibliografía
1. Alberts B, Johnson A, J. L, M. R, K. R, P. W: Biología Molecular de la Célula. 5ª edn2010.
2. Davidson MH, Johnson J, Rooney MW, Kyle ML, Kling DF: A novel omega-3 free fatty acid formulation has dramatically improved bioavailability during a low-fat diet compared with omega-3-acid ethyl esters: the ECLIPSE (Epanova((R)) compared to Lovaza((R)) in a pharmacokinetic single-dose evaluation) study. J Clin Lipidol 2012, 6:573-584.
3. Guyton AC, Hall JE: Tratado de Fisiología Médica. 13 edn: Elsevier; 2016.
4. Tresguerres A: Tratado de Fisiología Humana. 4ª edn: McGraw-hill; 2010.
5. Lawson LD, Hughes BG: Absorption of eicosapentaenoic acid and docosahexaenoic acid from fish oil triacylglycerols or fish oil ethyl esters co-ingested with a high-fat meal. Biochem Biophys Res Commun 1988, 156:960-963.
6. Lawson LD, Hughes BG: Human absorption of fish oil fatty acids as triacylglycerols, free acids, or ethyl esters. Biochem Biophys Res Commun 1988, 152:328-335.
7. Neubronner J, Schuchardt JP, Kressel G, Merkel M, von Schacky C, Hahn A: Enhanced increase of omega-3 index in response to long-term n-3 fatty acid supplementation from triacylglycerides versus ethyl esters. Eur J Clin Nutr 2011, 65:247-254.
8. Lembke P, Engelhardt H: SFE in sample preparation. Trends in Analytical Chemistry – TrAC 1994, 13.
9. Ruiz-Gayo M, Fernández-Alfonso M: Fundamentos de Farmacología Básica y Clínica. 2ª edn2013.